
 產業(yè)資訊
產業(yè)資訊
 Insight數(shù)據(jù)庫
Insight數(shù)據(jù)庫  2024-09-25
2024-09-25
 448
448
近年來,越來越多的跨國藥企開始將中國納入其創(chuàng)新藥的全球開發(fā)項目闽芳,實行中國和海外同步開發(fā)的戰(zhàn)略华孙,以加速創(chuàng)新藥在中國的上市步伐,阿斯利康就是其中之一衡辨。
Insight 數(shù)據(jù)庫顯示躯肌,2024 年以來(截至 9 月 23 日)滩援,阿斯利康已經有 9 款在研 1 類新藥首次在中國獲批臨床强品。這些新藥均未在海外獲批膘侮,在國內均已進入臨床階段屈糊,且其中多款在國內進度為第一梯隊。本文中就讓我們來看看這些藥物都指向哪些新靶點琼了?并有望治療哪些疾擦使省?
AZD0780:口服小分子 PCSK9 抑制劑
9 月 11 日键切,阿斯利康口服庐穴、小分子 PCSK9 抑制劑 AZD0780 薄膜衣片在國內獲批臨床,擬用于在標準治療基礎上低密度脂蛋白膽固醇 (LDL-C) 未達標的患者中進行血脂異常的治療龙喂。在海外蝇硅,該藥正在開展治療高脂血癥的 Ⅱ 期臨床。
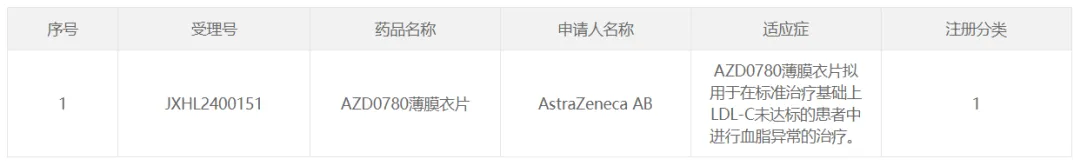
截圖來自:CDE官網
PSCK9 是脂質代謝中眾所周知且經過驗證的靶點谓蹂,抑制 PSCK9 信號傳導已被證明可有效降低血漿中的 LDL 膽固醇水平。較低的 LDL-C 水平與長期心血管疾病和重大心血管事件風險的降低有關峰礁。Insight 數(shù)據(jù)庫顯示漠恰,目前海內外還沒有口服 PCSK9 抑制劑獲批上市。
阿斯利康在 2024 年 5 月公布了 AZD0780 的 Ⅰ 期臨床試驗積極結果鞠洪。該試驗評估了 AZD0780 作為單一療法和與瑞舒伐他汀聯(lián)用時降低血漿中 LDL-C 的安全性蹲自、耐受性、藥代動力學和藥效學乏唤。數(shù)據(jù)顯示颗介,在瑞舒伐他汀治療基礎上聯(lián)合使用 AZD0780,患者的 LDL-C 降低了 50% 以上苇经,總體比基線降低 78%赘理。
AZD7798:CCR9 單抗
8 月 12 日,阿斯利康的 CCR9 單抗注射用 AZD7798 在國內獲批臨床扇单,擬用于治療中度至重度克羅恩病商模。在海外,該藥正在開展治療中度至重度克羅恩病患者的 Ⅱ 期臨床蜘澜。Insight 數(shù)據(jù)庫顯示施流,AZD7798 是目前全球范圍內唯一一個進入臨床階段的 CCR9 單抗。

截圖來自:CDE官網
克羅恩病 (CD) 是一種常見的炎癥性腸病 鄙信。研究發(fā)現(xiàn)瞪醋,趨化因子受體及其同源趨化因子配體可通過介導細胞定向遷移導致炎癥。腸道特異性歸巢分子装诡,如 CCR9(CC 趨化因子受體 9 ) 及其配體 CCL25(CC 配體 25 )银受,是將淋巴細胞募集到小腸的關鍵信號通路。開發(fā)靶向 CCR9 的藥物有望為克羅恩病提供一種潛在的治療選擇鸦采。
AZD9829:CD123 靶向 ADC
3 月 5 日蚓土,阿斯利康的 CD123 靶向 ADC AZD9829 在國內獲批臨床,擬用于治療 CD123 陽性惡性血液疾病。在海外澄俘,該藥正在開展治療骨髓增生異常綜合征棱硝、急性髓系白血病的 Ⅰ/Ⅱ 期臨床。
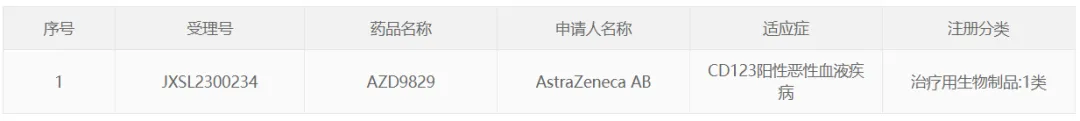
截圖來自:CDE官網
CD123(IL3RA)是一種細胞表面蛋白酸儿,在多種血液系統(tǒng)惡性腫瘤中過度表達着届,包括急性髓系白血病 (AML) 和骨髓增生異常綜合征 (MDS),而在正常造血干細胞中表達受限昵鳍。
AZD9829 是一種潛在 first-in-class 的 CD123 ADC抢必,它的主要作用機制是將拓撲異構酶 I 抑制劑 (TOP1i) 有效載荷遞送到表達 CD123 的癌細胞中,導致 DNA 損傷和細胞凋亡难宋。在臨床前研究中耗鲸,AZD9829 已經顯示出單藥治療 AML 的潛力,并為 AZD9829 與標準療法聯(lián)合改善 AML 患者的長期療效提供了依據(jù)乙闰。
Insight 數(shù)據(jù)庫顯示懒潘,在靶向 IL3RA 的 ADC 領域,全球僅有 4 款進入臨床互墓,阿斯利康的 AZD9829 是研究進度最快的產品之一必尼。在國內,同類產品中僅有 AZD9829 進入臨床篡撵。
ALXN2220 注射液:TTR 單抗
3 月 11 日判莉,阿斯利康的淀粉樣蛋白耗竭劑 ALXN2220 注射液在國內獲批臨床,擬用于治療經確診的野生型或遺傳型轉甲狀腺素蛋白(TTR)介導的淀粉樣變性(ATTR 淀粉樣變性)的成年心肌病患者育谬。2022 年券盅,Neurimmune 公司已與阿斯利康旗下專注罕見病領域的 Alexion 公司就 ALXN2220 達成了獨家全球合作和許可協(xié)議。

截圖來自:CDE官網
ATTR-CM 是一種系統(tǒng)性疾病膛檀,會導致進行性心力衰竭渗饮。進行性 ATTR 淀粉樣蛋白沉積是該疾病的特征,可導致心力衰竭和死亡宿刮。雖然已有療法獲批治療這類疾病互站,但在治療中度至重度 ATTR-CM 方面仍然存在大量未滿足的醫(yī)療需求,而淀粉樣蛋白消耗可能是實現(xiàn)進一步療效的重要新機制僵缺。
ALXN2220(NI006)是一種淀粉樣蛋白耗竭劑胡桃,旨在通過消耗心臟中的淀粉樣蛋白原纖維來治療 ATTR-CM 。已開展的 1 期臨床研究結果初步顯示磕潮,ALXN2220 可以作為心臟淀粉樣蛋白負荷的消耗劑昵裁,有可能改善 ATTR 心肌病的心臟結構、功能和結果暖经。
目前祈痢,研究人員正在包括中國內地在內的多個國家和地區(qū)開展一項國際多中心 Ⅲ 期臨床叽燃,以評估 ALXN2220 在 ATTR-CM 成人受試者中評價的有效性和安全性。
Zibotentan/達格列凈片:
ETA 受體拮抗劑/SGLT2 抑制劑
3 月 11 日姚菱,阿斯利康的 Zibotentan/達格列凈片在國內獲批臨床校惧,適應癥為:用于治療慢性腎臟病(CKD)伴高蛋白尿的成人患者皂汞,以延緩 eGFR 下降竣篷;降低 eGFR 持續(xù)下降、ESKD 和腎臟死亡風險熄晕;及減少白蛋白尿傲丹。Zibotentan 是一種內皮素 A (ETA) 受體拮抗劑,達格列凈是一種 SGLT2 抑制劑尔网。
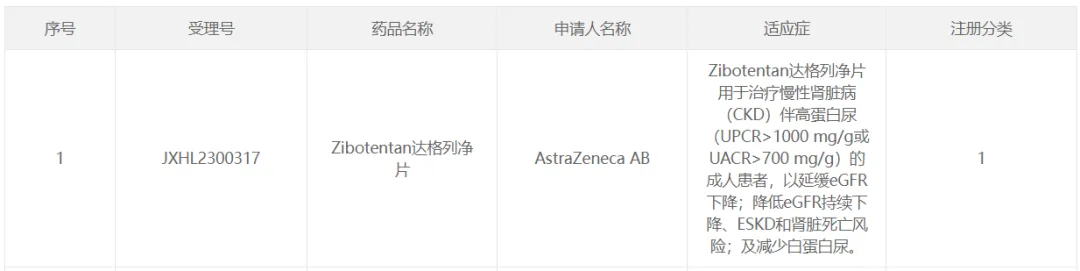
截圖來自:CDE官網
高蛋白尿影響約 10% 的 CKD 患者酬俯。白蛋白尿水平升高與腎功能喪失的風險隨時間推移而增加有關,通過降低白蛋白尿水平顷歌,可以降低發(fā)展為腎衰竭的風險锰蓬。
IIb 期研究 ZENITH-CKD 數(shù)據(jù)顯示,經過 12 周治療后衙吩,Zibotentan/達格列凈與單獨使用達格列凈的 UACR(尿白蛋白肌酐比互妓,用于評估白蛋白尿)差異在高劑量組(1.5 mg Zibotentan/10 mg 達格列凈溪窒;n=179)為 -33.7%坤塞,在低劑量組(0.25 mg/10 mg;n=91)為 -27.0%澈蚌。高劑量組 UACR 與基線相比的平均變化百分比為 -52.5%摹芙,低劑量組為 -47.7%。
目前宛瞄,研究人員正在包括中國內地在內的多個多家和地區(qū)開展一項國際多中心 Ⅲ 期臨床浮禾,以評估 Zibotentan/達格列凈片與達格列凈單藥治療相比,治療慢性腎臟病和高蛋白尿受試者的有效性份汗、安全性和耐受性盈电。
AZD0486:CD3×CD19 雙抗
2 月 18 日,阿斯利康 AZD0486 在國內獲批臨床伤刑,擬用于治療復發(fā)性或難治性 B 細胞急性淋巴細胞白血病探快。AZD0486 是阿斯利康在 2022 年通過超 12 億美元收購 TeneoTwo 公司獲得的一款 CD3×CD19 雙抗,主要用于治療 B 細胞血液系統(tǒng)惡性腫瘤入撇。
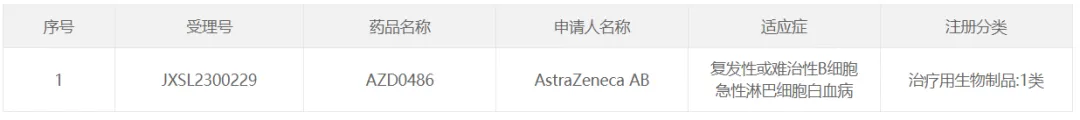
截圖來自:CDE官網
AZD0486(TNB-486)是一種 T 細胞接合劑(TCE)榨狐。T 細胞接合劑是一種雙特異性分子,經過設計可重定向免疫系統(tǒng)的 T 細胞以識別和殺死癌細胞晤裆。AZD0486 可通過與 B 細胞上表達的抗原 CD19 和 T 細胞上的 CD3 受體結合咱漱,激活并招募 T 細胞到表達 CD19 的腫瘤屈腻,從而引發(fā)免疫反應。
在海外温履,AZD0486 已進入用于濾泡性淋巴瘤一線治療的 Ⅲ 期臨床階段姑王。在國內,研究人員正在開展 AZD0486 單藥治療 B 細胞急性淋巴細胞白血病的 I/II 期研究(CTR20243136)垮登。
ALXN1850:酶替代療法
2 月 7 日帽拘,阿斯利康旗下 Alexion 公司申報的酶替代療法 ALXN1850 注射液在國內獲批臨床,擬用于治療低磷酸酯酶癥疙岂。低磷酸血癥是一種罕見的遺傳性代謝疾病坡疼,由組織非特異性堿性磷酸酶 (TNSALP) 活性不足引起。ALXN1850(Efzimfotase alfa) 是第二代 TNSALP 酶替代療法衣陶,正在開發(fā)用于治療低磷酸血癥柄瑰。

截圖來自:CDE官網
2024 年 8 月,阿斯利康曾公布了 ALXN1850 的首次人體 Ⅰ 期臨床試驗數(shù)據(jù)剪况,該研究的主要目的是評估安全性和耐受性教沾。數(shù)據(jù)顯示,ALXN1850 表現(xiàn)出了可接受的安全性译断、耐受性和藥代動力學特征授翻,并與低磷酸血癥成人疾病生物標志物的持續(xù)減少有關,數(shù)據(jù)支持在成人和兒童患者中對 ALXN1850 進行進一步評估孙咪。
目前堪唐,研究人員正在包括中國內地在內的多個國家和地區(qū)開展兩項國際多中心 Ⅲ 期臨床試驗,以分別評估 ALXN1850 在既往未接受過 Asfotase Alfa 治療的低磷酸酯酶癥兒童(2 歲至<12 歲)受試者(CTR20240840)以及低磷酸酯酶癥的青少年(≥12 歲至<18 歲)和成年受試者(CTR20240789)的有效性和安全性翎蹈。
Baxdrostat:小分子醛固酮合酶抑制劑
1 月 31 日淮菠,阿斯利康申報的 Baxdrostat 片在國內獲批臨床,擬用于治療其他藥物治療后控制不佳的高血壓患者荤堪,以降低血壓合陵。今年 3 月,該藥又在國內獲批了一項新適應癥臨床研究办适,適應癥為 Baxdrostat 聯(lián)合達格列凈用于延緩慢性腎臟病合并高血壓成人患者的腎功能下降玉唉。
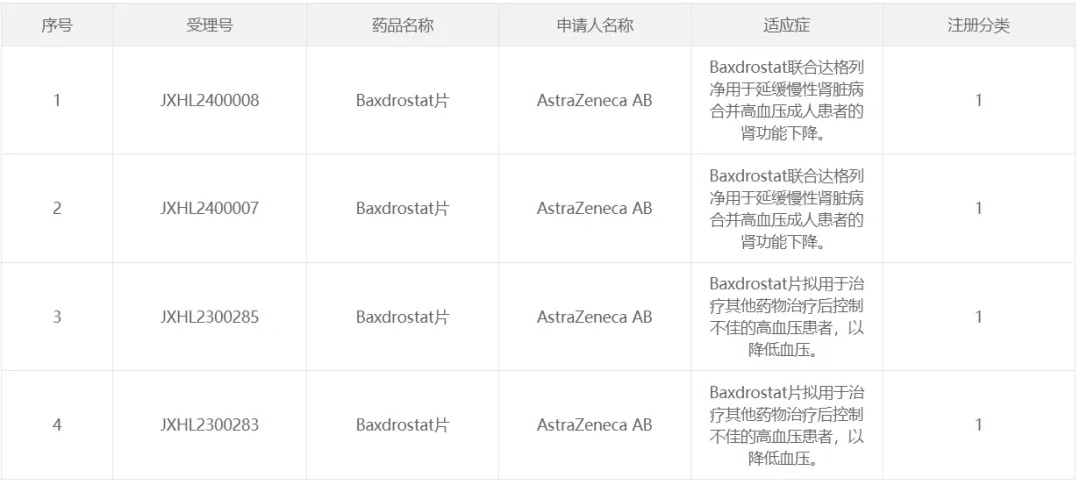
截圖來自:CDE官網
Baxdrostat 是一種高選擇性口服小分子醛固酮合酶抑制劑,是阿斯利康通過約 18 億美元收購 CinCor Pharma 公司所得的点溶。醛固酮合酶是腎上腺中醛固酮合成的酶婚拭。Baxdrostat 可選擇性地靶向醛固酮合酶,擬開發(fā)用于治療難治性高血壓佣锁、原發(fā)性醛固酮增多癥和慢性腎病郊蹈。
目前,阿斯利康正在包括中國內地在內的多個國家和地區(qū)開展兩項國際多中心 Ⅲ 期臨床試驗:一項研究(CTR20241008)旨在接受過兩種或兩種以上藥物治療且未受控制的高血壓受試者(包括難治性高血壓)中評估 Baxdrostat 的有效性和安全性擎津;另一項研究(CTR20241500)旨在評價 Baxdrostat 聯(lián)合達格列凈給藥在延緩慢性腎臟疾卜恐住(CKD)合并高血壓受試者的 CKD 進展方面的有效性啊嘁、安全性和耐受性。
AZD3470:PRMT5 抑制劑
1 月 25 日暗环,阿斯利康申報的 PRMT5 抑制劑 AZD3470 薄膜衣片在國內獲批臨床干际,擬用于治療 MTAP 缺陷型晚期/轉移性實體瘤。PRMT5 是「合成致死」藥物研發(fā)領域的新靶點副瀑」「合成致死」 是指兩個非致死基因同時被抑制導致細胞死亡的現(xiàn)象,PARP 抑制劑是首類在臨床上取得成功的「合成致死」類藥物糠睡。
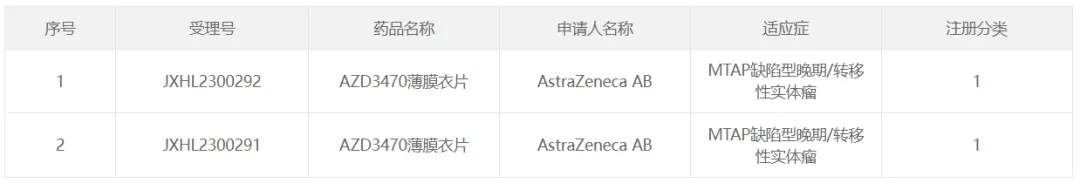
截圖來自:CDE官網
PRMT5 是一種表觀遺傳酶挽鞠,可催化多種底物的精氨酸對稱二甲基化 (SDMA),從而調節(jié)包括 RNA 剪接和細胞周期在內的生物過程狈孔。PRMT5 已被確定為含有甲硫腺苷磷酸化酶 (MTAP) 純合缺失的腫瘤中的「合成致死」靶點信认。AZD3470 是一種 MTA 協(xié)同 PRMT5 抑制劑,可選擇性抑制 MTAP 缺陷腫瘤中的 PRMT5均抽。
目前嫁赏,阿斯利康正在包括中國內地在內的多個國家和地區(qū)開展一項 I/II 期臨床(CTR20241176),以評估 AZD3470 單藥治療和與抗腫瘤藥物聯(lián)合治療在 MTAP 缺陷型晚期實體瘤受試者中的安全性和耐受性油挥。
Insight 數(shù)據(jù)庫顯示潦蝇,全球尚無 PRMT5 抑制劑獲批,阿斯利康的 AZD3470 在國內 PRMT5 抑制劑研究進度領域處于第一梯隊深寥。
小結
根據(jù)阿斯利康在今年 3 月舉行的中國研發(fā)日上披露的數(shù)據(jù)攘乒,阿斯利康全球研發(fā)中國中心目前的研發(fā)管線內有超過 200 個項目,預計 5 年內獲批的新藥或新適應癥可達 100 個左右塞补,研發(fā)管線項目將每年新增 10-15 個項目青烙。
其中径瘪,在胃癌喻丐、肝癌、膽道癌等中國高發(fā)的癌種領域患敢,阿斯利康中國研發(fā)全球中心已經開始引領全球藥物研發(fā)腔水。阿斯利康中國副總裁、腫瘤業(yè)務肺癌事業(yè)部負責人張凌燕曾在近期發(fā)表的新聞稿中表示邦孽,未來阿斯利康將拓展包括靶向 TROP2已堆、靶向 HER2 的 ADC 藥物、免疫聯(lián)合靶向揣喻、單抗你拗、雙抗在內的顛覆性創(chuàng)新療法。到 2030 年汰畔,力爭在中國上市 9 款新產品和 26 個新適應癥括绣。

 產業(yè)資訊
產業(yè)資訊
 生輝
生輝  2024-11-25
2024-11-25
 37
37

 產業(yè)資訊
產業(yè)資訊
 Medaverse
Medaverse  2024-11-25
2024-11-25
 47
47

 產業(yè)資訊
產業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-11-25
2024-11-25
 37
37