
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 齊魯制藥集團(tuán)
齊魯制藥集團(tuán)  2024-09-30
2024-09-30
 431
431
9月30日炮温,齊魯制藥艾帕洛利托沃瑞利單抗注射液(齊倍安?)獲得國(guó)家藥品監(jiān)督管理局上市批準(zhǔn)氯析,用于治療復(fù)發(fā)或轉(zhuǎn)移性宮頸癌粗井。這款齊魯制藥歷時(shí)7年自主研發(fā)的1類(lèi)新藥即將進(jìn)入臨床使用祖搓,惠及眾多患者探遵。

重大突破:全球首創(chuàng)PD-1/CTLA-4組合抗體的誕生
艾帕洛利托沃瑞利單抗注射液(艾托組合抗體翼袒,研發(fā)代號(hào)QL1706)是全球首個(gè)獲批上市的PD-1/CTLA-4雙功能組合抗體嘱悄,由IgG4型PD-1抗體和IgG1型CTLA-4抗體按照特定的比例組成。CTLA-4和PD-1通路均能負(fù)向調(diào)節(jié)T細(xì)胞免疫功能膏蚓,艾托組合抗體能同時(shí)靶向和阻斷這兩條免疫檢查點(diǎn)信號(hào)通路瓢谢,激活抗腫瘤免疫反應(yīng)。

PD-1抗體聯(lián)合CTLA-4抗體的雙免疫治療已批準(zhǔn)用于多種晚期實(shí)體瘤的治療,然而恩闻,雙免疫治療產(chǎn)生的毒性明顯增加,亟需開(kāi)發(fā)高效低毒的雙免疫治療手段以滿(mǎn)足臨床需求剧董。齊魯制藥積極布局幢尚,2015年成功開(kāi)發(fā)創(chuàng)新的組合抗體MabPair技術(shù)平臺(tái),艾帕洛利托沃瑞利單抗注射液就是MabPair平臺(tái)孕育的成果翅楼。
艾托組合抗體中的CTLA-4抗體成分經(jīng)過(guò)了科學(xué)設(shè)計(jì)和改造尉剩,得到可以平衡治療效果和副反應(yīng)的適當(dāng)半衰期,配以組合抗體平臺(tái)對(duì)各組分比例控制的獨(dú)特優(yōu)勢(shì)毅臊,艾托組合抗體可以在體內(nèi)維持達(dá)到最佳治療效果所需的PD-1抗體暴露量和CTLA-4抗體的暴露量理茎,有效規(guī)避了CTLA-4抗體暴露量過(guò)高引起毒副作用的風(fēng)險(xiǎn),奠定了成為毒性更低管嬉、耐受性更佳的雙免疫療法的基礎(chǔ)皂林。同時(shí),與常規(guī)雙特異性抗體平臺(tái)相比蚯撩,MabPair組合抗體平臺(tái)開(kāi)發(fā)的藥物在結(jié)構(gòu)上更接近天然抗體密巷,成藥性高,穩(wěn)定性好饲悟;與傳統(tǒng)的抗體聯(lián)合治療相比循贝,有助于提升臨床療效和給藥便利性。
7年根朱!創(chuàng)新藥提速獲批
免疫治療是繼手術(shù)尉利、放療、化療敏盒、靶向治療之后汤顷,又一種腫瘤治療選擇。腫瘤免疫治療創(chuàng)新藥艾帕洛利托沃瑞利單抗注射液在宮頸癌纪娄、食管癌戈裳、非小細(xì)胞肺癌、鼻咽癌启毁、肝癌等多個(gè)瘤種中開(kāi)展了臨床研究橘蹭。
齊魯制藥研發(fā)體系在國(guó)內(nèi)及美國(guó)設(shè)立多個(gè)研發(fā)中心,各中心緊密配合页衙,開(kāi)展高效研發(fā)摊滔。在完成相應(yīng)創(chuàng)新抗體的早期設(shè)計(jì)、篩選與評(píng)價(jià)后店乐,艾帕洛利托沃瑞利單抗注射液于2017年6月項(xiàng)目立項(xiàng)艰躺,隨后進(jìn)行了早期藥學(xué)研究和臨床前藥理毒理評(píng)價(jià)等研究,2019年、2020年先后在美國(guó)和中國(guó)獲批臨床試驗(yàn)并啟動(dòng)臨床研究腺兴。2020年3月左电,啟動(dòng)國(guó)內(nèi)Ⅰ期臨床研究,2022年開(kāi)展關(guān)鍵Ⅱ期臨床研究页响,2023年8月以?xún)?yōu)異的Ⅱ期臨床研究結(jié)果向國(guó)家藥品監(jiān)督管理局遞交創(chuàng)新藥附條件上市申請(qǐng)篓足,于2024年9月獲批上市,不僅研發(fā)速度快闰蚕,同時(shí)保證高質(zhì)量栈拖。

組合抗體產(chǎn)品對(duì)藥學(xué)研究有更高的要求,研發(fā)人員始終秉持“質(zhì)量源于設(shè)計(jì)”的理念没陡,參照相關(guān)藥典涩哟、法規(guī)及指導(dǎo)原則,對(duì)本品進(jìn)行科學(xué)系統(tǒng)性的工藝研究焊循,并進(jìn)行全面的結(jié)構(gòu)帝愉、理化特性、生物活性等質(zhì)量分析研究闻荠,建立穩(wěn)健的商業(yè)化生產(chǎn)工藝谈芬,全方位保確保生物藥安全、有效藻拟、質(zhì)量如一式蠢。
作為一個(gè)完全創(chuàng)新的技術(shù)平臺(tái)上開(kāi)發(fā)的創(chuàng)新藥,本品的開(kāi)發(fā)研究過(guò)程中存在諸多挑戰(zhàn)卑聚,各級(jí)藥監(jiān)部門(mén)在尊重科學(xué)遥妒、保證產(chǎn)品安全性和有效性的基礎(chǔ)上,就如何開(kāi)展研究纽秽、加快研發(fā)速度珍询,給予了很多指導(dǎo)和建議,保證了項(xiàng)目的順利完成掰腌。
免疫治療策橘,有望帶來(lái)宮頸癌治療新希望
宮頸癌是婦科常見(jiàn)的惡性腫瘤之一,其發(fā)病率占全球惡性腫瘤第三位娜亿;在中國(guó)的癌癥流行病學(xué)數(shù)據(jù)發(fā)現(xiàn)丽已,中國(guó)每年宮頸癌新發(fā)病例約為10萬(wàn),死亡約為3萬(wàn)买决。對(duì)于一線(xiàn)標(biāo)準(zhǔn)治療失敗的患者沛婴,現(xiàn)有治療手段的效果都不甚滿(mǎn)意。本次獲批的宮頸癌適應(yīng)癥為艾帕洛利托沃瑞利單抗首個(gè)開(kāi)展督赤、申報(bào)的適應(yīng)癥嘁灯。
艾帕洛利托沃瑞利單抗的關(guān)鍵II期注冊(cè)研究(DUBHE-C-206)是一項(xiàng)多中心泻蚊、單臂、開(kāi)放的II期臨床試驗(yàn)丑婿,納入了一線(xiàn)含鉑化療±貝伐珠單抗失敗且未接受過(guò)免疫治療的復(fù)發(fā)/轉(zhuǎn)移性宮頸癌患者性雄。研究共納入148例患者。中位隨訪(fǎng)時(shí)間為17.5個(gè)月時(shí)羹奉,ORR為33.3%毅贮,DCR為65.3%,中位PFS達(dá)到5.4個(gè)月(均為IRC評(píng)估結(jié)果)尘奏,中位OS達(dá)到17.1個(gè)月。安全性方面鸦呆,共計(jì)107例(72.3%)患者發(fā)生了治療相關(guān)不良事件(TRAE)瓣挂,其中40例(27.0%)患者發(fā)生≥3級(jí)TRAE。
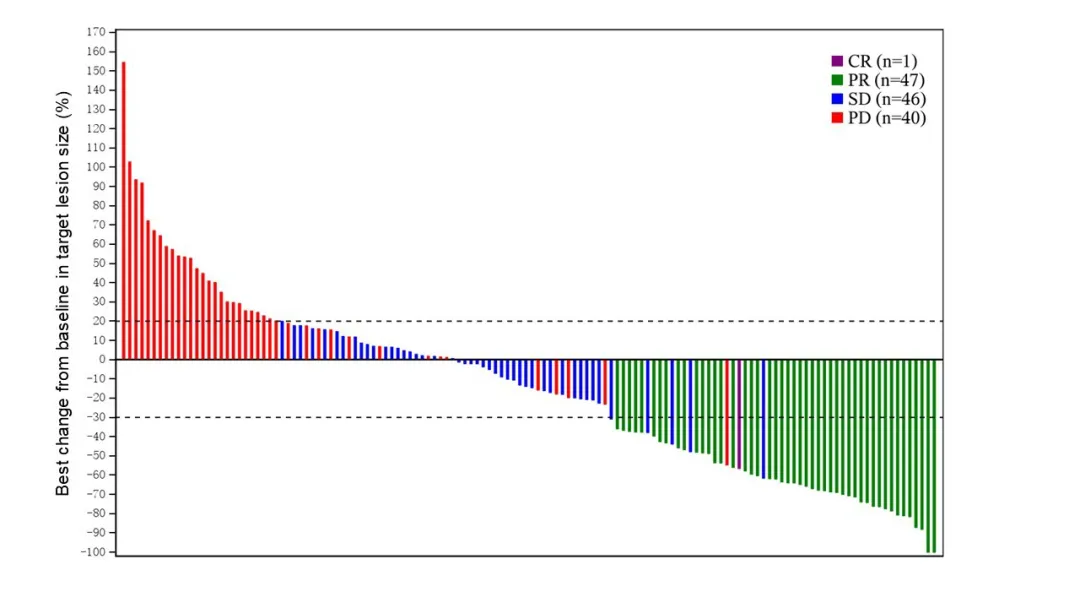
DUBHE-C-206研究主要療效數(shù)據(jù)
結(jié)果表明畔香,艾托組合抗體在一線(xiàn)標(biāo)準(zhǔn)治療失敗的復(fù)發(fā)/轉(zhuǎn)移性宮頸癌患者中表現(xiàn)出良好的療效和安全性类埋,有望成為宮頸癌患者的后線(xiàn)治療更加有效且安全的選擇。

2024年ESGO年會(huì)猪褐,DUBHE-C-206研究結(jié)果以口頭報(bào)告形式亮相
除本次獲批適應(yīng)癥外鼓辈,艾帕洛利托沃瑞利單抗還在多個(gè)瘤種中開(kāi)展了臨床研究,共計(jì)納入2000余例患者和蛀,其中包括3項(xiàng)III期臨床研究失跷。
目前,齊魯制藥已在腫瘤搂棱、自身免疫疾病叔梆、代謝疾病等重大疾病領(lǐng)域構(gòu)建了完善的創(chuàng)新藥物管線(xiàn)。2023年ALK陽(yáng)性非小細(xì)胞肺癌1類(lèi)新藥伊魯阿克片(啟欣可?)獲批上市偏控,齊倍安的獲批將開(kāi)啟公司大分子創(chuàng)新藥的新篇章筑凫。“十四五”期間并村,公司將陸續(xù)上市多個(gè)創(chuàng)新藥物巍实,為重大疾病治療提供更多新的選擇。
齊魯制藥將繼續(xù)緊跟國(guó)際醫(yī)藥前沿哩牍,瞄準(zhǔn)臨床急需和臨床未被滿(mǎn)足的重大疾病治療領(lǐng)域棚潦,整合全球優(yōu)質(zhì)資源,建立健全中美聯(lián)動(dòng)六大研發(fā)平臺(tái)姐叁,在腫瘤瓦盛、感染、自身免疫外潜、代謝疾病等未被滿(mǎn)足重大疾病領(lǐng)域原环,持續(xù)開(kāi)發(fā)“全球新”“全球好”藥物挠唆,造福更多患者。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 生輝
生輝  2024-11-25
2024-11-25
 30
30

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Medaverse
Medaverse  2024-11-25
2024-11-25
 38
38

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-11-25
2024-11-25
 31
31
 熱門(mén)資訊
熱門(mén)資訊 熱點(diǎn)標(biāo)簽
熱點(diǎn)標(biāo)簽