
 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥經(jīng)濟報
醫(yī)藥經(jīng)濟報  2024-10-11
2024-10-11
 320
320
國產(chǎn)PD-1抑制劑正加速進軍國際市場溅宅。
日前研铆,百濟神州宣布其PD-1抑制劑替雷利珠單抗(美國商品名:TEVIMBRA)在美國正式商業(yè)化上市拉盘,用于治療既往接受過系統(tǒng)化療(不含PD-1/L1抑制劑)后不可切除或轉(zhuǎn)移性食管鱗狀細胞癌(ESCC)的成人患者鄙骏。

全球藥企都將美國市場視為出海的必爭之地绒怯。2023年10月底搬即,君實生物的特瑞普利單抗(美國商品名:LOQTORZI)獲得FDA批準坑搀,成為首款在美國上市的鼻咽癌藥物,也是FDA批準上市的首個來自中國的生物創(chuàng)新藥和PD-1抑制劑贿桃。2024年3月溜封,百濟神州的替雷利珠單抗緊隨其后,在美國獲批首個適應癥裹视。
在獲得FDA批準六個多月后踢寂,替雷利珠單抗終于在美國正式實現(xiàn)上市銷售。在業(yè)內(nèi)看來缠黍,君實生物弄兜、百濟神州等中國藥企不斷拓展國際市場,反映了國產(chǎn)PD-1藥物技術(shù)的不斷成熟以及企業(yè)日益增長的全球野心瓷式。未來替饿,PD-(L)1抑制劑賽道將吸引更多參與者,但競爭將不再局限于國內(nèi)市場贸典,而是朝著國際化盛垦、全球化的方向發(fā)展。
價格低于競品10%
又一國產(chǎn)PD-1在美入市
由于各國創(chuàng)新藥定價體系存在差異瓤漏,一款創(chuàng)新藥進入不同的市場會根據(jù)當?shù)氐氖袌鲶w系進行定價。據(jù)了解颊埃,百濟神州將替雷利珠單抗的定價較其他獲批用于該適應癥的PD-1療法降低了10%蔬充,以提高藥品可及性。據(jù)報道班利,百濟神州的一位發(fā)言人透露饥漫,替雷利珠單抗的平均批發(fā)采購價估計為每月15075美元(約10.63萬元人民幣)。
上述其他獲批用于該適應癥的PD-1療法包括默沙東的Keytruda(帕博利珠單抗罗标,俗稱“K藥”)和百時美施貴寶的Opdivo(納武利尤單抗拍斜,俗稱“O藥”)。據(jù)悉过拿,規(guī)格為100mg/4ml的K藥在美國售價為4800美元(約3.3萬元人民幣)惹炕;規(guī)格為240mg的O藥在美國的定價大約是6500美元(約4.6萬元人民幣)。
在業(yè)內(nèi)看來祸铁,替雷利珠單抗在美定價低于同類產(chǎn)品睦氧,目的可能是想以低價爭奪市場。此外秦谁,臨床獲益程度也是決定新藥定價的因素之一世砰。替雷利珠單抗在美批準上市是基于RATIONALE 302試驗結(jié)果,該試驗在意向性治療(ITT)人群中達到了主要終點以称。
與化療相比友合,替雷利珠單抗展現(xiàn)了具有統(tǒng)計學顯著性和臨床意義的生存獲益论赋。但K藥和O藥占領(lǐng)美國市場由來已久,具有先發(fā)優(yōu)勢颊夷,其他后來者或許只有憑借低價進入市場才能贏得一線生機牌辛。
作為百濟神州兩大核心自研產(chǎn)品之一,替雷利珠單抗為其貢獻了不少業(yè)績瑞你。2024年第二季度酪惭,替雷利珠單的銷售額為1.58億美元,同比增長6%者甲,上半年總計達3.03億元春感,同比增長14.9%。替雷利珠單抗銷售額的提升虏缸,主要得益于新適應癥納入醫(yī)保所帶來的新增患者需求以及藥品進院數(shù)量的增加鲫懒。目前,替雷利珠單抗在中國獲批13項適應癥刽辙,11項適應癥已納入國家醫(yī)保目錄窥岩,廣泛覆蓋肺癌、肝癌等中國高發(fā)癌種宰缤。
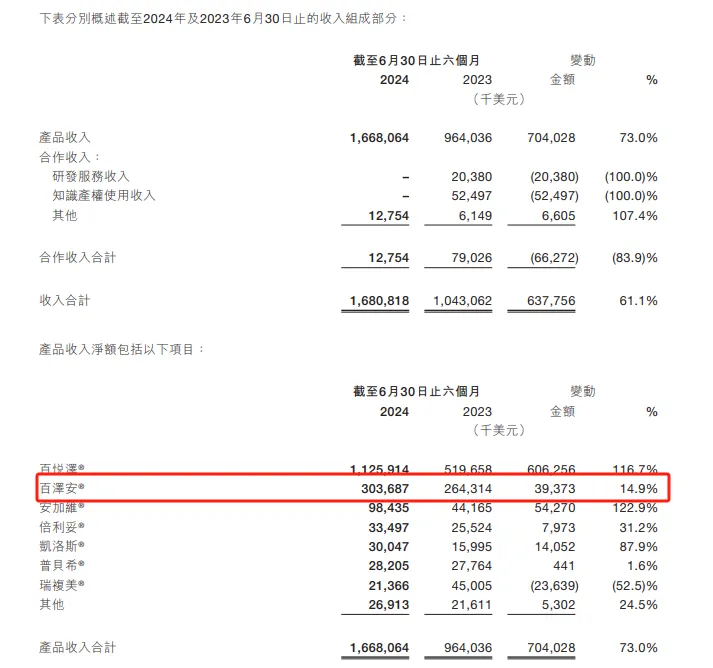
與亮眼的財報數(shù)據(jù)相比颂翼,替雷利珠單抗進軍美國市場的道路并非一帆風順。
早在2021年1月慨灭,百濟神州與諾華就替雷利珠單抗在全球多個國家的開發(fā)朦乏、生產(chǎn)與商業(yè)化達成了合作與授權(quán)協(xié)議,總交易金額達22億美元慢夸,創(chuàng)下了當時國內(nèi)單藥授權(quán)交易金額最高紀錄罗炸。同年9月,百濟神州便向FDA遞交了替雷利珠單抗二線治療ESCC的上市申請咕菱,PDUFA日期為2022年7月12日么歹。
不過,疫情的突襲阻斷了替雷利珠單抗在美國的上市進程珍喘。2022年7月14日晚間殿潜,百濟神州發(fā)布公告稱,因疫情相關(guān)旅行限制等因素性谬,F(xiàn)DA無法如期在中國完成所需的現(xiàn)場核查工作疫橘,因此將延長替雷利珠單抗新藥上市許可申請(BLA)的目標審評完成時間。
面對變幻莫測的國際市場和競爭格局匾颁,百濟神州的合作伙伴諾華改變想法癌玩。2023年9月,百濟神州突然發(fā)布公告稱,公司決定終止與諾華的海外授權(quán)交易污益,重新獲得了替雷利珠單抗的全球開發(fā)桃熄、生產(chǎn)和商業(yè)化權(quán)利。一紙合同的終止型奥,意味著百濟神州將獨自負責在美國開展替雷利珠單抗上市相關(guān)的業(yè)務(wù)瞳收。
歷時近兩年,替雷利珠單抗終于在2024年3月叩開了美國FDA的大門厢汹。這也是繼君實生物之后螟深,第二個成功出海美國的國產(chǎn)PD-1產(chǎn)品。有業(yè)內(nèi)人士認為烫葬,美國市場PD-1藥物的市場規(guī)模約500億美元界弧,國產(chǎn)PD-1藥物成功進入這一市場,意味著能夠分享到巨大的市場蛋糕搭综。替雷利珠單抗在美國的上市垢箕,不僅對百濟神州的商業(yè)發(fā)展具有重要意義,也對推動中國創(chuàng)新藥物的國際化進程和全球患者治療選擇具有積極影響兑巾。
本土藥企加速進軍歐美
下一個會是恒瑞条获?
公開數(shù)據(jù)顯示,過去五年間蒋歌,全球PD-(L)1抑制劑的市場表現(xiàn)引人注目罪焰,其復合年增長率達到了45%,是整體腫瘤市場增長率的三倍风承。隨著PD-(L)1抑制劑市場的不斷成熟佩捎,預計未來其復合年增長率放緩至15%。有機構(gòu)預測刑评,到2025年,全球PD-(L)1抑制劑銷售額將增至580億美元灭奉,盡管這一增長率相對較低且恼,但仍高于整體腫瘤市場預期的10%復合年增長率。
盡管全球市場規(guī)模相當可觀过任,但PD-(L)1抑制劑賽道的市場競爭仍然激烈捉寻。截至2024年上半年,中國已有15款PD-(L)1抑制劑藥物獲批上市江眯。此外硼洁,國內(nèi)關(guān)于PD-1/PD-L1藥物的臨床試驗登記數(shù)量超過600條,涉及企業(yè)超過150家东摘,其中近200條已進入Ⅲ期臨床階段欢策。
已有PD-1產(chǎn)品的本土藥企,為了在市場中占據(jù)一席之地,正在尋求國際化發(fā)展并追求差異化踩寇。目前啄清,已有兩款國產(chǎn)PD-1藥物在歐美地區(qū)獲批上市,分別是百濟神州的替雷利珠單抗和君實生物的特瑞普利單抗俺孙。
值得一提的是辣卒,恒瑞醫(yī)藥的卡瑞利珠單抗有望成為繼君實生物和百濟神州之后,下一個實現(xiàn)美國上市銷售的國產(chǎn)PD-1藥物睛榄。
不過荣茫,恒瑞醫(yī)藥的卡瑞利珠單抗在美上市進程也遭遇不少挫折。今年5月场靴,恒瑞醫(yī)藥發(fā)布公告啡莉,收到FDA關(guān)于卡瑞利珠單抗聯(lián)合阿帕替尼用于不可切除或轉(zhuǎn)移性肝細胞癌患者一線治療的生物制品許可申請(BLA)的完整回復信(Complete Response Letter )。

回復信中憎乙,F(xiàn)DA表示會基于企業(yè)對生產(chǎn)場地檢查缺陷的完整答復進行全面評估票罐;并且由于部分國家的旅行限制,F(xiàn)DA表示在審查周期內(nèi)也無法全部完成該項目必需的生物學研究監(jiān)測計劃(BIMO)臨床檢查泞边。恒瑞醫(yī)藥彼時表示颖喧,公司計劃積極與FDA保持密切溝通,并盡快重新提交上市申請顾惹,以期產(chǎn)品能夠盡快在美國獲批上市铅坚。
據(jù)業(yè)內(nèi)人士了解,完整回復信也就是業(yè)內(nèi)通常所說的CRL,FDA會在其中詳細說明可能存有缺陷和風險厉亥,并提出建議方案兰斑,如果申請人能在規(guī)定時間內(nèi)完成更改,實際上并不影響最終批準藏趁。也就是說修暑,此次恒瑞卡瑞利珠單抗的美國上市程序僅是延遲。
在業(yè)內(nèi)看來谎雷,PD-1藥物的海外上市并不是終點奥唯,其商業(yè)化的成功和盈利能力同樣重要。
近期楚榕,君實生物的美國合作伙伴Coherus發(fā)布了2024年第二季度業(yè)績報告商贾。其中,與君實生物合作的君實PD-1特瑞普利單抗(Loqtorzi)在美國第二季度商業(yè)化銷售額為380萬美元吨拗,相較其第一季度200萬美元的凈銷售額放量增長90%满哪。
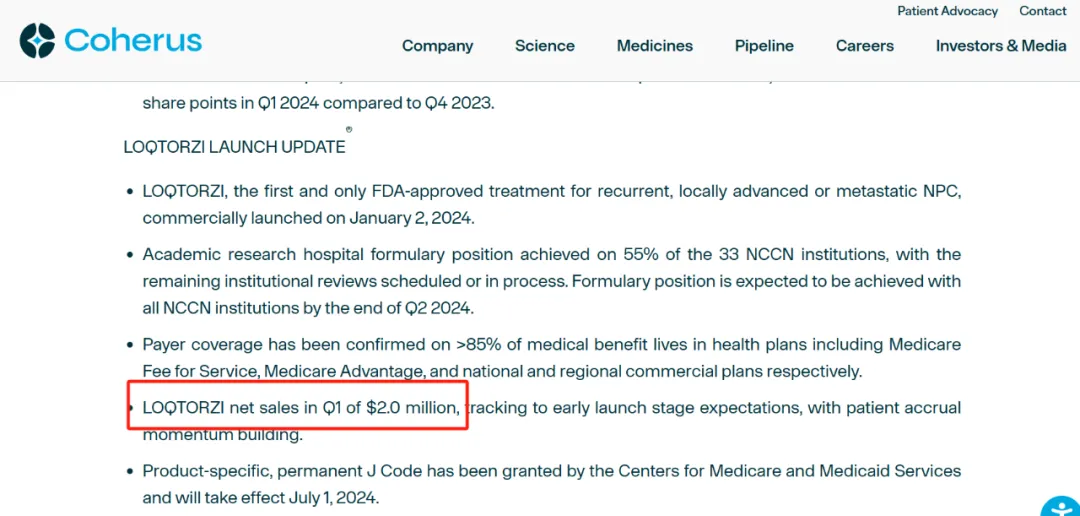
2024年初,Coheurs計劃專注于腫瘤微環(huán)境及與PD-1通路互補的高潛力產(chǎn)品線劝篷,特瑞普利單抗是與其新型藥物聯(lián)合研究的支柱哨鸭。Coheurs預計特瑞普利單抗在鼻咽癌單項適應癥中銷售峰值將達到2億美金,預計在2-3年達成;并且兔跌,到2032年特瑞普利單抗銷售額有望逼近20億美金勘高。

盡管Coheursu推進的特瑞普利單抗銷售額有所增長,但與預期的峰值銷售相比仍存在較大差距坟桅。這可能與特瑞普利單抗在美國獲批的適應癥——復發(fā)性华望、局部晚期或轉(zhuǎn)移性鼻咽癌(NPC)的患者人數(shù)較少有關(guān),其在美國的商業(yè)化進展還是較為緩慢仅乓,未來還有比較長的路要走赖舟。
隨著中國制藥企業(yè)在創(chuàng)新藥物研發(fā)領(lǐng)域取得顯著成就,國產(chǎn)PD-1藥物的國際化進程正在加速夸楣。這不僅滿足了制藥企業(yè)在商業(yè)層面的追求宾抓,也標志著其研發(fā)實力已達到全球先進水平,展現(xiàn)了中國制藥企業(yè)在全球醫(yī)藥產(chǎn)業(yè)中日益提升的影響力和競爭力忱确。

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 生輝
生輝  2024-11-25
2024-11-25
 26
26

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 Medaverse
Medaverse  2024-11-25
2024-11-25
 31
31

 產(chǎn)業(yè)資訊
產(chǎn)業(yè)資訊
 醫(yī)藥觀瀾
醫(yī)藥觀瀾  2024-11-25
2024-11-25
 26
26