
 研發(fā)追蹤
研發(fā)追蹤
 2016-08-25
2016-08-25
 5710
5710
來源:藥明康德??? 2016-08-25
禮來公司(EliLillyandCompany)和阿斯利康公司(AstraZeneca)今天宣布羽氮,美國FDA授予其在研新藥AZD3293快速通道資格,用于開發(fā)治療阿爾茨海默氏病。AZD3293是一款口服β-分泌酶裂解酶(BACE)抑制劑,目前正處于3期臨床試驗(yàn)。這款藥物在早期試驗(yàn)中已被證明可降低阿爾茲海默病及健康志愿者腦脊液中β-淀粉樣蛋白的水平遥巴。
阿爾茨海默氏癥是一種致命的疾病,也是失智癥類型疾病的最常見形式,占據(jù)病例的60%到80%汛欺。目前,國際阿爾茲海默病協(xié)會(huì)(Alzheimer'sDiseaseInternational)估計(jì)全世界范圍內(nèi)有4600萬人患有失智癥设塑,這個(gè)數(shù)字預(yù)計(jì)在2030年將增長到7400萬琉语,2050年將會(huì)達(dá)到1.31億狗丙。由于只有50%的患者曾經(jīng)接受了正規(guī)的診斷,阿爾茨海默氏病仍然是全球面臨的重大健康挑戰(zhàn)之一密哈。2015年扼褪,全世界因失智癥診療產(chǎn)生的總費(fèi)用估計(jì)為8180億美元。到2018年粱栖,失智癥將成為“1兆美元”的疾病话浇,2030年還會(huì)翻番到2兆美元。
與心臟疾病及癌癥不一樣闹究,自第一款治療藥物于1993年在美國獲批以來幔崖,阿爾茲海默病藥物研究沒有出現(xiàn)大的進(jìn)展。目前已有的阿爾茲海默病藥物只能暫時(shí)渣淤、最低限度地改善患者記憶及進(jìn)行日常行為的能力赏寇,但不能延緩疾病的進(jìn)程。
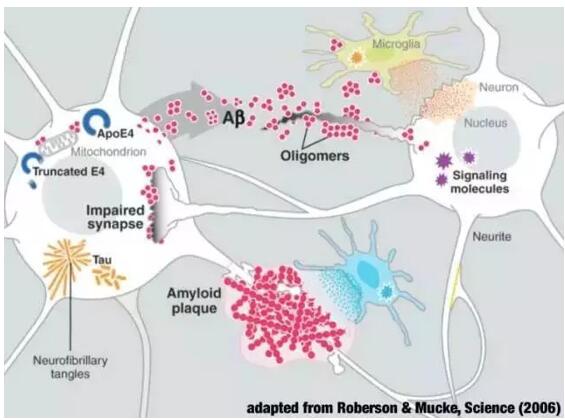
Aβ在大腦中沉積導(dǎo)致阿爾茨海默氏癥(圖片來源:CarnegieMellonUniversity)
目前大量醫(yī)學(xué)研究認(rèn)為价认,β淀粉樣蛋白(Aβ)在大腦中的沉積是導(dǎo)致阿爾茨海默氏癥的原因之一嗅定。依據(jù)這一致病機(jī)理,眾多學(xué)術(shù)研究機(jī)構(gòu)和生物制藥企業(yè)努力尋找能夠減少Aβ生成的新型藥物用踩,它們將不僅能改善癥狀渠退,還能夠減緩疾病的進(jìn)展。
β-分泌酶BACE是一種影響體內(nèi)Aβ生成的酶類脐彩。如果能控制住這個(gè)酶的活性论艰,就有望減少人體中Aβ的總量,便可銳減Aβ在腦中形成沉積的機(jī)會(huì)发刨,并最終起到延緩疾病進(jìn)展的效果勇袋。
?
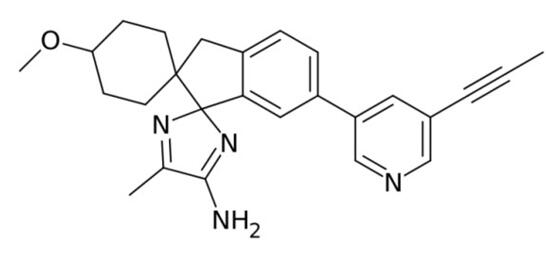
AZD3293的分子式(圖片來源:Wikipedia)
?
AZD3293是一種口服強(qiáng)效小分子BACE抑制劑,已在早期臨床試驗(yàn)中顯示出可降低阿爾茨海默病患者和健康志愿者腦脊液中的Aβ水平太队。
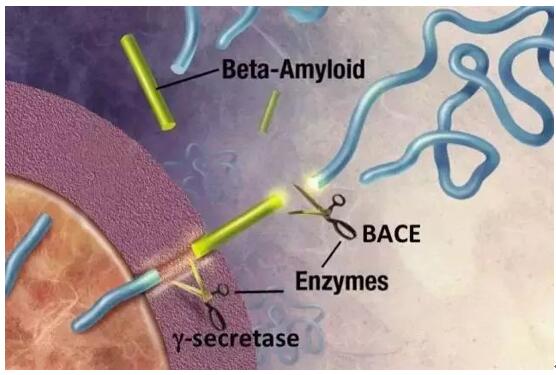
BACE與Aβ生成相關(guān)(圖片來源:CoMentis淑助,Inc.)
根據(jù)合作協(xié)議,禮來和阿斯利康兩家公司將共同開展II期和III期臨床試驗(yàn)痢玖。禮來將與阿斯利康的神經(jīng)科學(xué)創(chuàng)新藥物部門合作負(fù)責(zé)臨床研究工作光稽,而阿斯利康則將負(fù)責(zé)藥品的生產(chǎn)。兩家公司將共同負(fù)責(zé)今后所有的AZD3293研發(fā)和市場化工作砍没。除了繼續(xù)現(xiàn)有的2/3期研究外懒竖,禮來和阿斯利康還公布了第二項(xiàng)AZD3293的3期臨床計(jì)劃。該項(xiàng)被稱為DAYBREAK-ALZ的臨床研究擬評估AZD3293針對輕度阿爾茲海默病患者的安全性和有效性鸥司,并開始在2016年第三季度的招募參與者舅洋。
禮來副總裁兼全球阿爾茲海默病開發(fā)負(fù)責(zé)人PhyllisFerrell女士說道:“我們很高興美國FDA高度重視針對阿爾茨海默氏病的新藥研發(fā),這是我們這個(gè)時(shí)代最嚴(yán)峻的健康問題之一。這項(xiàng)快速通道資格認(rèn)定對數(shù)以百萬計(jì)的病人著摔、家屬缓窜、護(hù)理人員和醫(yī)師們來說,是非常積極的一步谍咆。”

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 114
114

 研發(fā)追蹤
研發(fā)追蹤
 醫(yī)藥魔方Info
醫(yī)藥魔方Info  2024-11-25
2024-11-25
 115
115

 研發(fā)追蹤
研發(fā)追蹤
 藥明康德
藥明康德  2024-11-25
2024-11-25
 114
114
 熱門資訊
熱門資訊